Иммунотерапия рака, такая как блокада иммунных контрольных точек (ICB), является революционным методом лечения опухолей, усиливая иммунный надзор и даже способствуя долгосрочному контролю над заболеванием.
В исследовании, опубликованном в журнале Nature Nanotechnology, группа исследователей во главе с Ли Япином и Чжан Пенгченг из Шанхайского института Materia Medica Китайской академии наук (CAS) продемонстрировала, что парадоксальные эффекты дополнительной терапии IFN могут быть устранены с помощью мембраны Т-лимфоцитов.
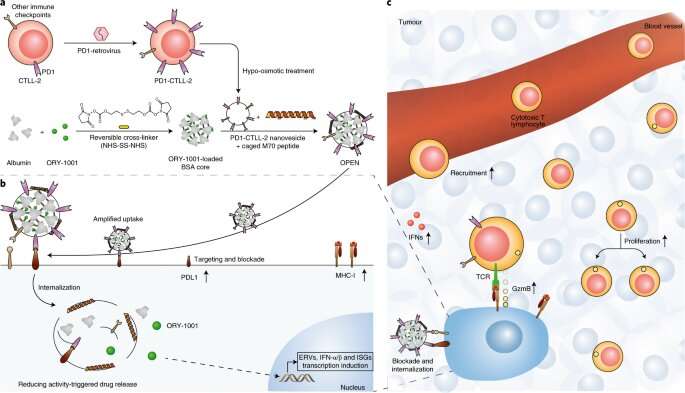
Сначала исследователи с помощью генной инженерии создали линию цитотоксических Т-клеток, сверхэкспрессирующую рецептор запрограммированной смерти 1 (PD1), а затем использовали мембрану этих клеток для оболочки белковой наночастицы, содержащей ORY-1001, ингибитор лизин-специфической гистоновой деметилазы 1 (LSD1), чтобы создать OPEN.
Они показали, что OPEN улучшили внутриопухолевое накопление ORY-1001 и местную продукцию IFN после внутривенного введения, и продемонстрировали, что IFN увеличивают инфильтрацию опухоли, пролиферацию и активность опухолеспецифических цитотоксических Т-клеток и отображение антигена опухолевых клеток.
Кроме того, они доказали, что IFN-индуцированный лиганд 1 запрограммированной смерти (PDL1) и другие молекулы иммунных контрольных точек легко нейтрализовались последующим OPEN. Этот последовательный процесс специфически восполнял внутриопухолевые IFN и ослаблял IFN-индуцированное уклонение от иммунитета и, таким образом, замедлял рост опухоли на множественных моделях опухолей.
«Исследование демонстрирует элегантную стратегию решения парадоксальных эффектов дополнительной терапии IFN с использованием эпигенетического наноиндуктора IFN. Это веха в области наномедицины для более безопасной и эффективной иммунотерапии рака», — сказал профессор Чжао Юйлян, академик CAS.
Источник — aobe.
