Группа ученых под руководством Эрика Сторкебаума из Института Дондерса Университета Радбауд расшифровала молекулярный механизм, лежащий в основе одной из форм периферической нейропатии Шарко-Мари-Тута (CMT). Это заболевание поражает как двигательные, так и чувствительные нервы. Этот научный прорыв предлагает новую форму лечения этой неизлечимой болезни. Их результаты будут опубликованы в Science 3 сентября.
Подтип CMT, изученный Сторкебаумом и его командой, встречается у одного из 100000 человек, что делает его довольно редким заболеванием. До сих пор ученые не были уверены в молекулярных механизмах этого заболевания, а эффективных лекарств пока нет.
У больных этим заболеванием поражаются как двигательные, так и сенсорные нервы, что приводит к мышечной слабости и сенсорным расстройствам. «Заболевание вызывает потерю чувствительности, например, под подошвами ступней, а также мышечную слабость, а также из-за высокой ступенчатой походки и деформации стопы. Болезнь прогрессирует медленно, но неуклонно, и пациенты часто оказываются в инвалидных колясках», — говорит ведущий исследователь Эрик Сторкебаум.
Мутации в шести генах
Мутации в шести генах, кодирующих тРНК-синтетазы, вызывают Шарко-Мари-Тута (CMT). тРНК-синтетазы связывают аминокислоты (строительные блоки белков) с их транспортной РНК (тРНК), что является важным первым шагом в производстве белка. В своих исследованиях ученые показывают, что CMT-мутантные версии одной такой тРНК-синтетазы (глицил-тРНК-синтетазы) все еще могут связывать свою тРНК, но не могут ее высвободить.
Этот «захват» глицил-тРНК истощает запас этой тРНК в клетке, что приводит к недостаточной доставке глицил-тРНК к рибосоме (молекулярной машине, производящей белки). Следовательно, рибосома перестает производить белки, когда достигает кодона аминокислоты глицина. Это нарушает производство белков и вызывает стрессовую реакцию клеток.
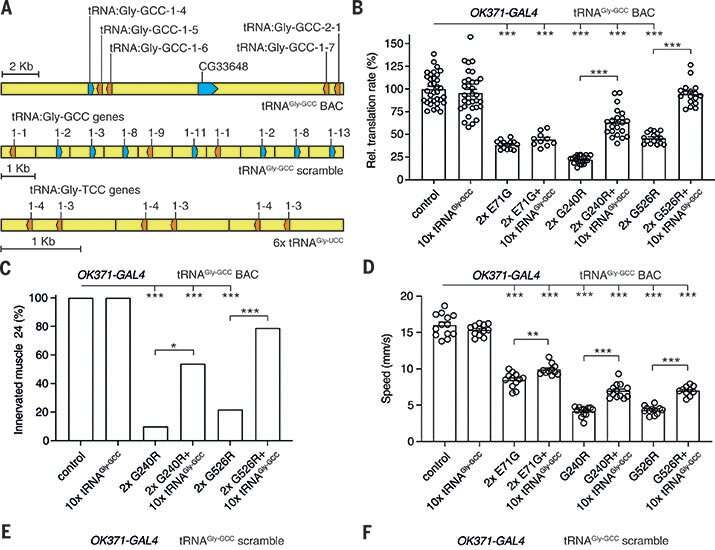
Ученые показывают, что увеличение количества глицил-тРНК у трансгенных животных может предотвратить периферическую невропатию и нарушить синтез белка у плодовых мух и мышей на моделях CMT, вызванных мутациями в глицил-тРНК синтетазе. Соответственно, повышение уровня глицил-тРНК у пациентов с этой формой ШМТ может быть разработано в качестве нового метода лечения этого неизлечимого заболевания.
Сторкебаум: «Сейчас мы раскрыли одну форму, но мы подозреваем, что есть еще пять форм CMT, основанных на аналогичном механизме, и поэтому их можно сопоставить». Эта форма CMT — первое нейродегенеративное заболевание, которое было обнаружено на молекулярном уровне и имеет путь к лечению. Теоретически такие болезни, как болезнь Паркинсона и Альцгеймера, можно было бы распознать аналогичным образом. «Так что это многообещающее открытие для будущего лечения других нейродегенеративных заболеваний».
Источник — aobe.
